
来源:壹财信
作者:赵鹤鸣
近年来,疫苗的安全问题越来越引起社会的广泛关注, 特别是长生生物因产品生产过程中存在记录造假的重大违法行为而被强制退市,使各地对于疫苗安全监管工作提出了更高的要求。
作为疫苗生产企业,北京万泰生物药业股份有限公司(下称:万泰生物)在安全生产等方面或也存在隐忧,旗下两家子公司去年在相关主管部门的现场检查时接连出现了问题,暴露了其在生产管理上的漏洞。
成立于1991年的万泰生物主要从事体外诊断试剂、体外诊断仪器与疫苗的研发、生产及销售,核心产品有艾滋病毒诊断试剂、病毒性肝炎系列诊断试剂、全自动管式化学发光免疫分析系统、重组戊型肝炎疫苗、人乳头瘤病毒系列疫苗、冻干水痘减毒活疫苗(VZV-7D)等。经过近三十年的发展,万泰生物已成为我国创新免疫诊断产品和创新疫苗研发的领先企业。
据万泰生物招股书,公司建立了健全的质量管理体系,在供应商资质管理、原材料采购、生产加工、产品试制、售后服务等环节制订了严格的质量管理规范,由各生产部门遵照执行。
但是,《壹财信》发现,万泰生物旗下两家子公司在执法部门的现场检查中接连被发现存在多个问题。
据福建省食品药品监督管理局于2019年7月29日发布的《关于"施爱德(厦门)医疗器材有限公司"等医疗器械生产企业"双随机一公开"检查结果公示》中,厦门万泰凯瑞生物技术有限公司(下称:万泰凯瑞,系万泰生物全资子公司)被现场检查出9项问题。
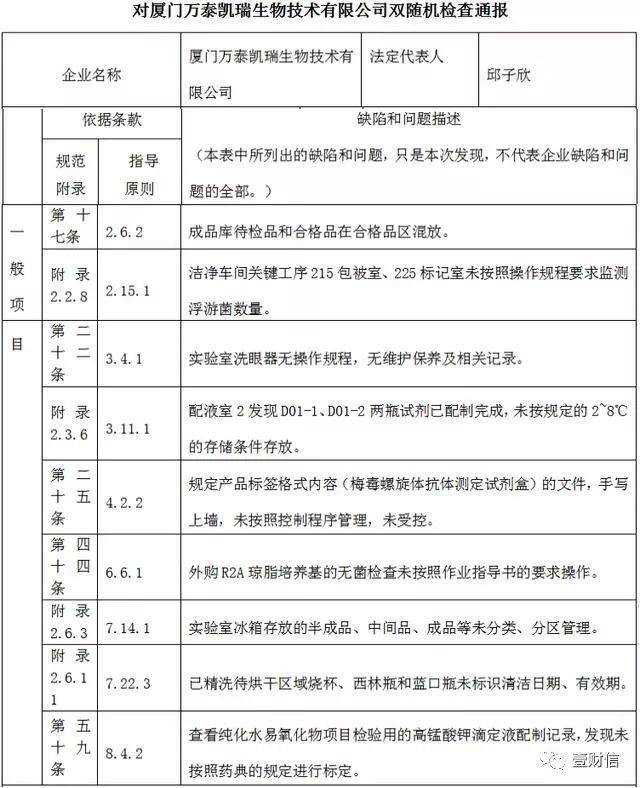
(截图来自福建省食品药品监督管理局官网)
针对现场检查中发现的问题,福建省药品监督管理局厦门稽查办督促万泰凯瑞限期整改,必要时跟踪复查,并要求万泰凯瑞评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》的规定召回相关产品。万泰凯瑞完成整改后,厦门稽查办应将相关情况通报省局医疗器械处。
此外,万泰生物的另一家控股子公司厦门优迈科医学仪器有限公司(下称:优迈科)也在执法部门的抽检中被发现存在问题。
据福建省食品药品监督管理局2019年12月4日发布的《关于"福安市格新医疗器械有限公司"等医疗器械生产企业"双随机一公开"检查结果公示》中,优迈科被现场检查出两项问题。
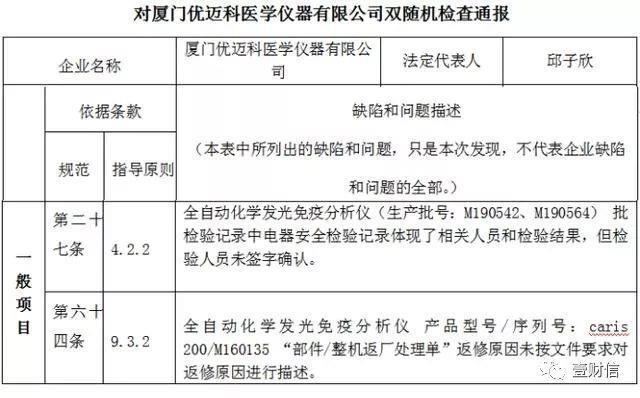
(截图来自福建省食品药品监督管理局官网)
据公开信息,万泰生物IPO已于2019年12月26日成功过会,其拟在上交所主板公开发行新股不超过4,360万股,募集资金3.8亿元,保荐机构为国金证券。
随后2019年12月31日,国家药监局批准了万泰生物全资子公司厦门万泰沧海生物技术有限公司的双价人乳头瘤病毒疫苗(商品名:馨可宁)的上市注册申请,这标志着首个国产宫颈癌疫苗即将投产上市。
顶着"首个国产宫颈癌疫苗"光环的万泰生物,或应加强对子公司的管理,避免再次出现上述问题,以确保产品质量,《壹财信》也将保持关注。
版权声明:
本网仅为发布的内容提供存储空间,不对发表、转载的内容提供任何形式的保证。凡本网注明“来源:XXX网络”的作品,均转载自其它媒体,著作权归作者所有,商业转载请联系作者获得授权,非商业转载请注明出处。
我们尊重并感谢每一位作者,均已注明文章来源和作者。如因作品内容、版权或其它问题,请及时与我们联系,联系邮箱:service@qeerd.com,投稿邮箱:tougao@qeerd.com